当地时间1月19日-21日,2023年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)在旧金山拉开帷幕。本次会议将讨论消化系统肿瘤领域最具创新性的科学进展。目前免疫治疗是
摘要358
INFINITY:一项多中心、单臂、多队列、II期试验,对高度微卫星不稳定性(MSI-H)可切除胃或胃食管交界腺癌(GAC/GEJAC)患者进行tremelimumab和
研究背景:在可切除的GAC/GEJAC中,MSI-H患者预后更佳,但无法从化疗中获益。鉴于MSI-H肿瘤对免疫疗法的高反应性,新辅助或明确的双重CTLA-4/PD(L)-1抑制可能避免化疗或手术。
研究方法:INFINITY是一项多中心、单臂、多队列II期试验(NCT04817826),旨在研究tremelimumab+度伐利尤单抗作为新辅助(队列1)或确定性(队列2)治疗MSI-H、错配修复缺陷(dMMR)和EBV阴性可切除GAC/GEJAC。在队列1中,患者接受为期12周的单次高剂量tremelimumab 300mg和度伐利尤单抗1500mg(T300/D),每4周一次,治疗3个周期,然后进行手术。主要终点是T300/D后ctDNA阴性的pCR率(ypT0N0)。次要终点包括无病生存期(DFS)、总生存期(OS)和生活质量。探索性包括pCR与临床变量的相关性、IHC22C3评估的PDL-1 CPS、FoundationOne检测的肿瘤突变负荷(TMB)、液体
研究结果:总体而言,队列1共纳入了18例MSI-H/dMMR可切除cT2-4任何NGAC/GEJAC患者。1例患者撤回了知情同意,2例患者在影像学和内窥镜检查(正在进行)中获得了完全的临床病理缓解,并拒绝手术。
在15例可评估的患者中,1例出现疾病进展,14例接受了切除术。pCR率为60%(9/15),主要病理学缓解率(<10%活细胞)为80%。所有pCR患者术前ctDNA状态均为阴性。T4肿瘤的pCR率为1/6(17%),T2-3肿瘤为8/9(89%)(p=0.011),而未发现pCR率与基线N状态相关。PD-L1CPS与结果无关,TMB与pCR的相关性趋势不明显(非pCR组的TMB中位数为26,pCR组为40,p=0.2)。
3例患者(n=18)发生≥3级免疫相关不良事件(AE):
研究结论:术前3个月的T300/D方案是安全的,并为MSI-H/dMMRGAC/GEJAC患者提供了有希望的疗效证据。这些结果为研究T300/D后临床、病理和分子(ctDNA微小残留病灶)完全缓解患者的非手术治疗策略开辟了道路。在独立数据监查委员会(IDMC)评估和协议之后,队列2的注册已经开始,修改为仅包含在分期
摘要364
PERSIST:围手术期奥沙利铂和S-1(SOX)联合或不联合
研究背景:RESOLVE研究表明,在接受D2胃切除术的局部晚期GC/GEJC患者中,围手术期SOX的改善具有临床意义。在化疗中加入PD-1抑制剂在晚期GC/GEJC的一线治疗中具有明显获益。在此,研究者比较了围手术期信迪利单抗联合SOX对比围手术期SOX在可切除的局部晚期GC/GEJC患者中的疗效。
研究方法:PERSIST是一项多中心、前瞻性、开放标签、随机对照的II期研究。具有组织学或细胞学证实的GC/GEJC、临床II-III期、既往未接受全身治疗、ECOG体能状态(PS)为0或1的患者符合入组条件。患者将被随机分配(1:1)接受围手术期信迪利单抗(200mg d1 Q3W,术前三个周期和术后长达1年)联合SOX(奥沙利铂130mg/m² d1,口服S-1 40–60mg BID d1-14 Q3W,试验组术前三个周期,术后五个周期)或对照组围手术期单独使用SOX。主要终点是完全病理缓解(pCR)率。次要终点是主要病理缓解(MPR)率、降期率、3年DFS率、5年OS率以及安全性。
研究结果:截至2022年9月,共有101例患者入组,中位年龄为61岁(范围31-75岁),男性85例(84.2%),cT2/3/4/X分别为2(2.0%)/5(5.0%)/93(92.1%)/1(1.0%),cN0/1/2/3/X分别为10(10.0%)/42(41.6%)/27(26.7%)/9(8.9%)/13(12.9%),GC/GEJC分别为92(91.1%)/9(8.9%)。47例(试验组26例,对照组21例)行根治性切除,均达到R0切除。
试验组和对照组的pCR率分别为26.9%和4.8%,MPR率分别为69.2%和28.6%。试验组和对照组分别有76.9%(20/26)和52.4%(11/21)的患者实现了降期。三例患者出现3-4级手术并发症。3-4级TRAE包括
研究结论:与单独使用SOX化疗相比,信迪利单抗联合SOX作为可切除局部晚期GC/GEJC的围手术期治疗获得了令人鼓舞的pCR率、MPR率和降期率,并且安全性可控。
摘要367
TQB2450联合
研究背景:晚期HER2阴性G/GEJ腺癌患者一线化疗的疗效和预后不佳。PD-1抑制剂联合化疗一线治疗G/GEJ腺癌疗效显著。TQB2450是一种创新型抗PD-L1单克隆抗体药物,在此,研究者探索了TQB2450联合安罗替尼以及CAPEOX(奥沙利铂+卡培他滨)作为晚期G/GEJ腺癌一线方案的疗效和安全性,并报告了初步结果。
研究方法:该研究招募了未接受过全身治疗的HER2阴性、不可切除的局部晚期或转移性G/GEJ腺癌患者。符合条件的患者接受TQB2450(1200mg,iv,d1,q3w)+安罗替尼(10mg,po,d1~14,q3w)联合奥沙利铂(130mg/m2,d1,iv,q3w)和卡培他滨(1000mg/m2,po,bid,d1~14,q3w)6个周期作为初始治疗。对于没有疾病进展(PD)的患者,采用TQB2450(1200mg,iv,d1,q3w)+安罗替尼(10mg,po,d1~14,q3w)维持治疗,直至出现PD或不可耐受的毒性。研究者根据RECIST1.1版使用CT扫描评估肿瘤反应。主要终点是客观缓解率(ORR),次要终点是缓解持续时间(DoR)、PFS、OS、疾病控制率(DCR)和安全性。
研究结果:2021年4月至2022年7月共入组20例可用于疗效评价。在最佳总体反应评估中,15例获得部分缓解(PR,75.0%)、4例达到疾病稳定(SD,20.0%),1例无法评估(NE,5.0%)。因此,初步ORR为75.0%(95%CI:50.9%~91.3%),DCR为95.0%(95%CI:75.1%~99.9%)。尚未达到中位PFS。此外,发生率>40%的最常见的治疗中出现的不良事件(AE)是血小板减少症(80%)、贫血(75%)、白细胞减少症(65%)、总蛋白减少(45%)。常见的≥3级治疗紧急不良事件是中性粒细胞减少(15%)、淋巴细胞计数减少(10%)、贫血(5%)、白细胞减少(5%)、天冬氨酸转氨酶升高(5%)和碱性磷酸酶升高(5%)。
研究结论:初步结果表明,TQB2450联合安罗替尼和CAPEOX一线治疗晚期G/GEJ腺癌表现出令人鼓舞的疗效和可控的不良事件,未来将在更大样本量中进一步验证。
参考文献:
1.INFINITY: A multicentre, single-arm, multi-cohort, phase II trial of tremelimumab and durvalumab as neoadjuvant treatment of patients with microsatellite instability-high (MSI) resectable gastric or gastroesophageal junction adenocarcinoma (GAC/GEJAC).2023 ASCO GI.Abstract 358.
2.PERSIST: A multicenter, randomized phase II trial of perioperative oxaliplatin and S-1 (SOX) with or without sintilimab in resectable locally advanced gastric/gastroesophageal junction cancer (GC/GEJC).2023 ASCO GI.Abstract 364.
3.Preliminary results of TQB2450 (PD-L1 blockade) plus anlotinib combined with oxaliplatin and capecitabine in the first-line treatment of advanced gastric or gastroesophageal junction (G/GEJ) adenocarcinoma: A single-arm, multicenter phase II clinical trial.2023 ASCO GI.Abstract 367.
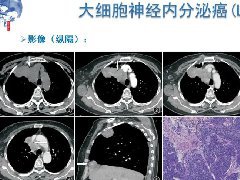 纵隔大细胞神经内分泌癌1例CT影像
纵隔大细胞神经内分泌癌1例CT影像 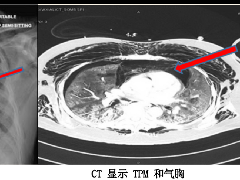 张力性纵隔气肿影像表现及严重度分级
张力性纵隔气肿影像表现及严重度分级 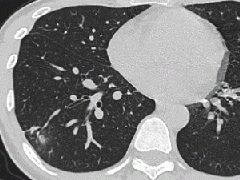 迅速增大的肺部结节,首先考虑良性,确诊需要肺穿
迅速增大的肺部结节,首先考虑良性,确诊需要肺穿 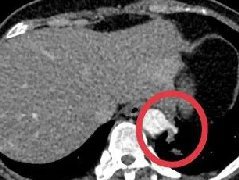 肺隔离症:易误诊为肺癌的占位性病变,肺穿刺禁忌!
肺隔离症:易误诊为肺癌的占位性病变,肺穿刺禁忌! 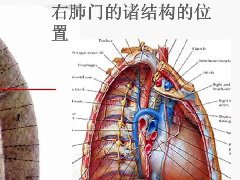 肺段与肺内管道应用解剖
肺段与肺内管道应用解剖 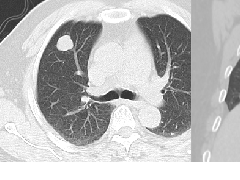 肺转移瘤的十种不典型CT表现
肺转移瘤的十种不典型CT表现 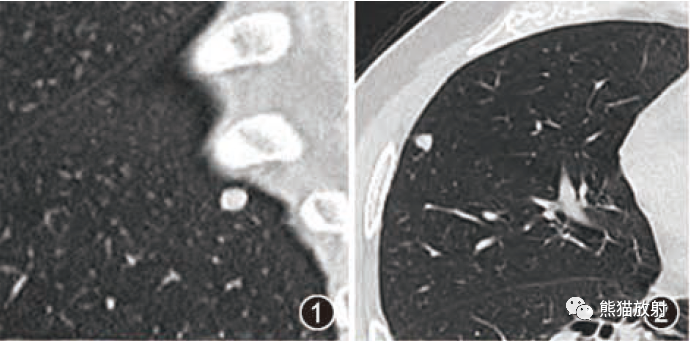 肺内淋巴结的CT表现特点及与病理对照
肺内淋巴结的CT表现特点及与病理对照  肺实变与肺不张的CT鉴别诊断
肺实变与肺不张的CT鉴别诊断  医生现身说法,这五种忙帮不得!
医生现身说法,这五种忙帮不得!  北大教授:要真正让医务人员有阳光体面的收入!医
北大教授:要真正让医务人员有阳光体面的收入!医  为值夜班的医生护士鼓与呼:请给我们更多关注!
为值夜班的医生护士鼓与呼:请给我们更多关注!  广东拟取消医院用药数量限制,满足患者多样性需求
广东拟取消医院用药数量限制,满足患者多样性需求  博士、硕士入职就给精装房!又有医院不惜下血本招
博士、硕士入职就给精装房!又有医院不惜下血本招  历时7年之久,温医生宣判无罪!
历时7年之久,温医生宣判无罪!  重磅!四川发文:严禁限制医生多点执业
重磅!四川发文:严禁限制医生多点执业  与真人医生诊断一致性达96%:AI医生应用前景广阔
与真人医生诊断一致性达96%:AI医生应用前景广阔