作者:王祥,王金梅,钟良,华中科技大学同济医学院附属武汉儿童医院麻醉科;杜艺敏,华中科技大学同济医学院附属同济医院护理部
气管破裂在平时并不多见,医源性气管破裂在临床上更加少见。气管破裂患者往往因为通气不足而出现低氧血症、高碳酸血症或其他致命性并发症,处理这种致命性损伤的方法是通过外科手术修补破裂气管或行气管重建术,术中如何维持患者的氧合对外科医生和麻醉医师提出了较高的要求。
根据破裂口的形态、大小、所在的位置(气管上段、气管中段、气管下端)不同,麻醉诱导的方法和术中的通气方式也不相同。麻醉医师需要根据患者的病情特点,通过术前评估制定个体化的麻醉诱导方案和术中通气策略,确保患者围手术期的生命安全。
1.临床资料
患儿,女,2岁3个月,身高93 cm,体重14 kg。患儿家属主诉为“发现纵隔囊肿2年余”。现病史:患儿在母亲孕期8个月时产检发现喉部阴影,考虑羊水影响,不排除食管囊肿可能,后未经处理继续观察。患儿于1个月前出现无明显诱因下
患儿在外院行CT检查提示:支气管炎、后纵隔囊行病变,气管远端及双主支气管明显受压。现患儿在安静时有阵发性刺激性咳嗽,未闻及明显痰音,无气促、喘息等不适,为求进一步诊治,患儿以“支气管炎”于2022年3月29日收入华中科技大学同济医学院附属武汉儿童医院心胸外科。患儿起病以来,精神食欲欠佳,二便正常,体重无明显变化。
1.1 患儿入院后查体
体温36.5 ℃,呼吸26次/分,脉搏124次/分,发育良好,神志清楚。专科查体:心前区无隆起,心尖冲动正常,心音正常,
术前心电图提示窦性心律,胸部X线片及
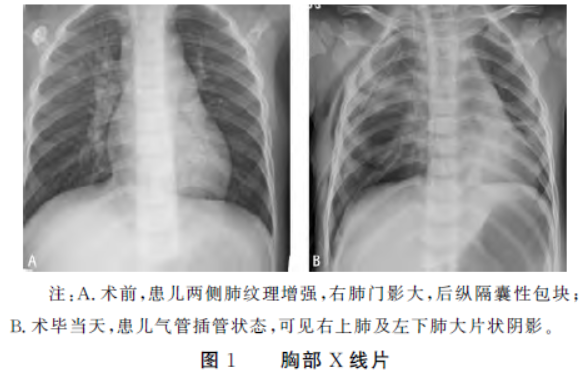
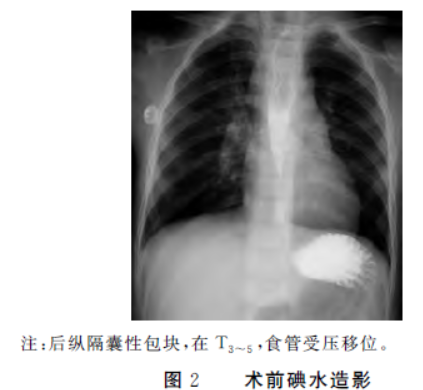
增强扫描后可见后纵隔病灶未强化,边界较平时清晰,病灶大小约34.9 mm×20.7 mm×40.9 mm,可见主动脉弓、奇静脉、降主动脉及左右肺动脉干环绕病灶。左主支气管明显受压,最窄处内径约1.9 mm。胸部CT检查诊断为:后纵隔囊性包块,前肠囊肿可能,双肺通气不均。术前检查完善后,拟择期行机器人辅助下后纵隔病损切除术。
1.2 麻醉及抢救过程
患儿入手术室后开放静脉通道,常规吸氧,行心电监护。采用快诱导麻醉,依次静脉推注异丙酚50 mg、芬太尼0.03 mg、罗库溴铵15 mg,待肌肉松弛药物起效后行气管插管,考虑患儿在左侧卧位下手术,麻醉医师试图将气管导管插入左侧主支气管进行单肺通气(OLV),用纤维支气管镜通过气管导管观察,可见左主支气管开口狭窄,纤维支气管镜无法通过,故放弃左侧OLV,遂将气管导管放在主气道,固定导管可见呼气末二氧化碳(PaCO2)波形良好。
术中使用持续泵注异丙酚10 mg/(kg·h)复合
在胸腔内置入达芬奇机器人相关器械,术中可见囊性包块位于奇静脉与上腔静脉之间,大小约为5 cm×5 cm×5 cm,位于食管前方,用电凝钩切开表面囊肿胸膜并逐步剥离囊肿,术中可见气管壁受压明显伴部分软化,左主支气管近隆突处尤甚。手术进行约半小时后,忽见麻醉机报警提示通气不足,不见PaCO2波形。
遂继出现血氧饱和度(SpO2)下降、血压(BP)下降、心率(HR)下降。立刻呼叫上级医生及麻醉科主任,考虑术中在剥离囊肿时出现了气管破裂。外科医生紧急开胸行气管修补术,由于破裂口在隆突附近,术前未能进行OLV,即麻醉机通过气管导管的气体可通过破裂口漏出而无法进行有效通气。
BP最低下降至40/20 mm Hg(1 mm Hg=0.133 kPa),静脉推注肾上腺素0.3 mg,持续泵注
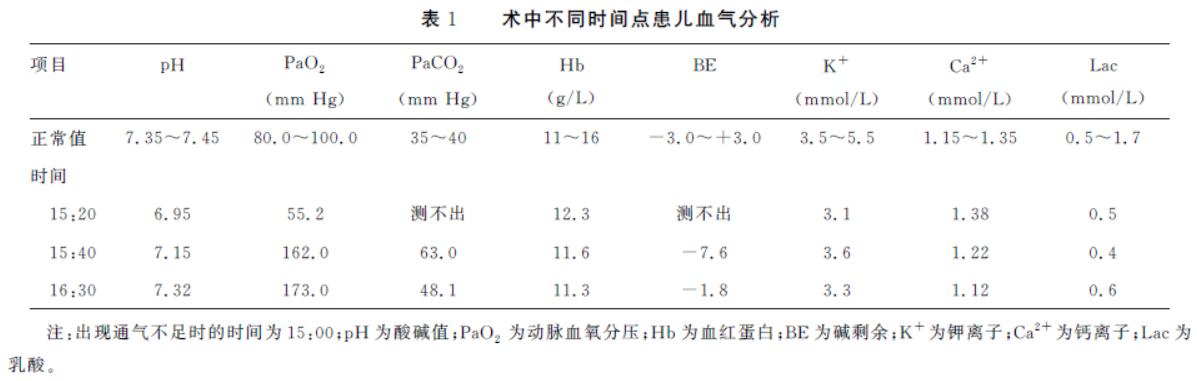
在5~10 min内,外科医生完成开胸下气管修补,后可见PaCO2波形逐渐正常,SpO2也逐渐恢复正常。泵注
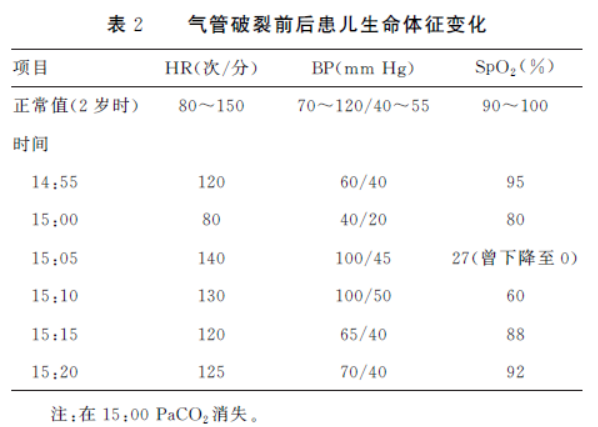
术毕麻醉医师吸痰、膨肺,带气管导管送入重症监护室(ICU)。入ICU后,继续予患儿镇静,于术后当天行床旁胸部X线片(图1B)提示:纵隔囊肿术后改变,两侧肺纹理增强,右上肺及左下肺可见斑片状模糊影,右侧胸腔及右侧胸壁可见气体影。术毕复查血常规提示红细胞计数3.80×1012 L-1,白细胞计数32.73×1012 L-1,血小板计数375×109 L-1,中性粒细胞百分比84.7%。肝功能、肾功能、电解质、凝血功能结果大致正常。患儿于第2天拔除气管导管,生命体征平稳,术后无不良并发症发生。
2.讨论
气管破裂通常由创伤性、医源性和自发性破裂引起,术中气管破裂是一种罕见但严重的并发症,可由胸部手术、气管插管或气管切开等造成,临床上可表现为氧合不足、痰中带血、皮下气肿等,严重时危及生命。在术中出现气管支气管破裂时的征象为麻醉机提示通气不足、PaCO2消失、SpO2下降等。需要注意术中PaCO2监测是瞬时监测,对于病情变化快的小儿手术尤为重要。
在术中PaCO2消失时,要考虑“DOPE四要素”即管道异位-Displacement、管腔堵塞-Obstruction、气胸-Pneumothorax、机器故障-Equipment failure。术中听诊两肺呼吸音或者术中行肺超声有助于鉴别诊断PaCO2消失的原因。通过围手术期肺超声检查,可以观测到肺滑移征、A线、B线、肺点等,能鉴别出肺不张、气胸、胸腔积液等。
在气管支气管破裂的情况下,麻醉管理的要点是确保足够的通气和维持氧供需平衡。在这种情况下,可能遇到的气体交换明显不足、血流动力学不稳定、修复病变部位操作困难等。传统的气管插管通气和间歇正压通气会导致漏气,以致通气不足或潮气量减少。因此,术中需要用双腔管或支气管封堵器控制呼吸。
目前,在OLV术中实行肺隔离技术的方法有支气管插管、支气管封堵器、双腔管插管、Univent管等,对于小儿则更多选择支气管封堵器实行肺隔离。剖胸和侧卧位对患者的呼吸和循环产生剧烈影响,尤其在小儿OLV中,更容易出现低氧血症和高碳酸血症。通过纤维支气管镜引导进行健侧支气管维持通气,术中行保护性肺通气策略,在确保通气情况下为外科医生提供手术条件。
对于操作难度大的气管修补术,可以参照气管肿瘤切除术的气道管理,即在手术台上由术者插入单腔气管导管至手术对侧主支气管内行OLV,在完成气管修补术后拔除在术野插入的气管导管,同时将经口插入的气管导管插入至吻合口下方进行通气,还可在手术台上用2台麻醉机行双肺分开通气进而维持氧合。
对于术中难以维持氧合或手术操作极其困难的患者,可以选择在体外循环或借助体外膜氧合(ECMO)技术进行气管修补术。术前可以在局部麻醉下选择股-股动静脉转流或ECMO,使术中难以维持氧合的患者平稳度过麻醉诱导期和手术环节。
对于难以维持氧合的患者,缺氧时间延长会导致多器官缺血、缺氧,严重时可出现心博骤停,需要立即进行心肺复苏。在胸腔镜术中可以紧急开胸后进行心脏按压,同时使用心血管药物或者电除颤来维持循环稳定,同时注意重要脏器包括对心、肺、脑的保护。
结合该病例,胸腔镜术中突发气管破裂在临床上比较罕见,主要是病变部位包绕隆凸,且合并气管软化情况,在分离囊肿过程中出现气管破裂这种急危重症。在胸腔镜术中且在机械通气状态下,出现气管破裂的征象是PaCO2消失,麻醉机提示通气不足,后续便出现SpO2下降。缺氧会引起重要脏器功能的失调,如出现心肌缺血、心律失常、脑卒中等,严重时可出现心博骤停。
幸运的是,该患儿出现气管破裂时正好处于胸腔镜术中,外科医生能快速进胸行气管修补术,且患儿一直处于气管插管状态,通过气管导管持续高流量给氧,为抢救患儿脱离持续低氧血症争取时间。该病例中,患儿取右侧卧位进胸,在隆凸处出现气管破裂,麻醉医师试图通过纤维支气管镜将气管导管插深至右肺进行右侧OLV,但右侧主支气管恰好被病变囊肿压迫致使气管导管通过受阻,所以在出现气管破裂时只能任通过气管导管的气流从破裂口漏出。
通过手动控制呼吸,加大氧流量,敦促外科医生快速修补气管破裂口,同时泵注心血管活性药物维持循环稳定,放置冰帽、给予激素及利尿剂进行脑保护,保证重要脏器尤其是心、肺、脑的血液灌注,延长重要脏器缺氧的时间。若由于缺氧出现心博骤停,则可以直接在开胸状态下进行心脏按压,或直接在手术台上进行支气管插管,通过破裂口实施单肺通气后继续给氧。
若气管破裂口较大或难以维持氧合状态,在有条件状态下可以采用ECMO技术,或者在体外循环下进行气管修补,或者行气管重建术。术毕患儿带气管导管入ICU,待患儿生命体征平稳及各项生理反射恢复后拔除气管导管,进行后续治疗。
综上所述,对于气管破裂的患者,麻醉医师对于气道的管理取决于气管破裂所在的位置。如果诊断为气管破裂,最好使气管导管前端超过破裂口;如果是隆凸附近或支气管破裂,则可以将单腔管插入未受累的支气管,也可以插入支气管封堵器或双腔管进行控制呼吸。
纤维支气管镜检查在确定破裂口或者引导支气管插管时非常有临床价值,在复苏过程中要时刻关注患者的生命体征,缩短低氧血症发生的时间,以及重要脏器尤其是心肺脑缺氧缺血的时间,通过多学科合作挽救患者的生命。
来源:王祥,王金梅,钟良等.机器人辅助下胸腔镜术中突发气管破裂1例[J].现代医药卫生,2023,39(03):537-540.
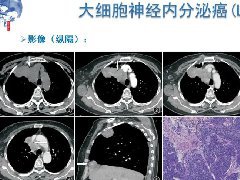 纵隔大细胞神经内分泌癌1例CT影像
纵隔大细胞神经内分泌癌1例CT影像 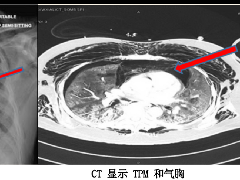 张力性纵隔气肿影像表现及严重度分级
张力性纵隔气肿影像表现及严重度分级 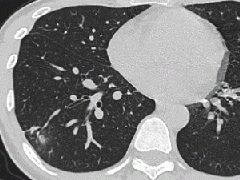 迅速增大的肺部结节,首先考虑良性,确诊需要肺穿
迅速增大的肺部结节,首先考虑良性,确诊需要肺穿 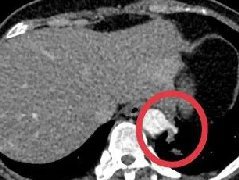 肺隔离症:易误诊为肺癌的占位性病变,肺穿刺禁忌!
肺隔离症:易误诊为肺癌的占位性病变,肺穿刺禁忌!  肺段与肺内管道应用解剖
肺段与肺内管道应用解剖  肺转移瘤的十种不典型CT表现
肺转移瘤的十种不典型CT表现  肺内淋巴结的CT表现特点及与病理对照
肺内淋巴结的CT表现特点及与病理对照 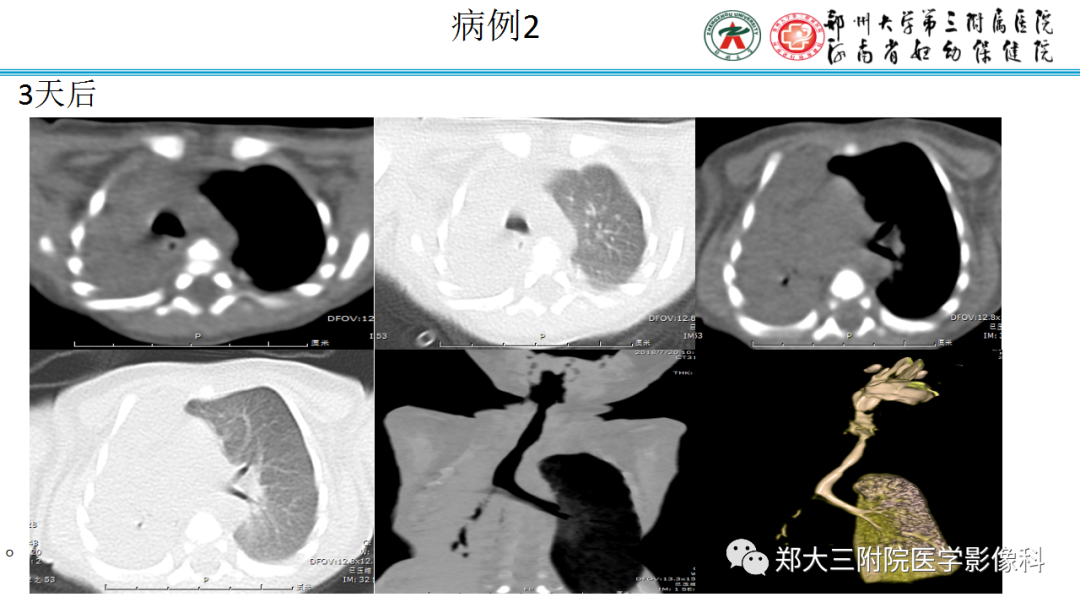 肺实变与肺不张的CT鉴别诊断
肺实变与肺不张的CT鉴别诊断  医生现身说法,这五种忙帮不得!
医生现身说法,这五种忙帮不得!  北大教授:要真正让医务人员有阳光体面的收入!医
北大教授:要真正让医务人员有阳光体面的收入!医  为值夜班的医生护士鼓与呼:请给我们更多关注!
为值夜班的医生护士鼓与呼:请给我们更多关注!  广东拟取消医院用药数量限制,满足患者多样性需求
广东拟取消医院用药数量限制,满足患者多样性需求  博士、硕士入职就给精装房!又有医院不惜下血本招
博士、硕士入职就给精装房!又有医院不惜下血本招  历时7年之久,温医生宣判无罪!
历时7年之久,温医生宣判无罪!  重磅!四川发文:严禁限制医生多点执业
重磅!四川发文:严禁限制医生多点执业  与真人医生诊断一致性达96%:AI医生应用前景广阔
与真人医生诊断一致性达96%:AI医生应用前景广阔 
