作者:张益益,杨玥怡,上海交通大学医学院附属第九人民医院口腔医学院;琚梧桐,钟来平,上海交通大学医学院附属第九人民医院口腔颌面-头颈肿瘤科
口腔鳞状细胞癌(口腔鳞癌)是口腔癌中最常见的病理类型,约占90%。其中约60%的口腔鳞癌患者在就诊时已处于临床晚期(TNM分期Ⅲ、Ⅳ期),预后较差,临床晚期的5年生存率仅有30%~40%。在NCCN(2021)指南中,对于可切除的Ⅲ/ⅣA期口腔鳞癌,推荐的治疗方案是以手术为主的综合治疗,或者进入临床试验。将患者纳入设计科学、流程完善的临床试验,可能有利于提高生存率和患者的生活质量。
本文报道上海交通大学医学院附属第九人民医院一项新辅助治疗前瞻性临床试验中的2例病例,其中1例达到病理完全缓解(pCR);1例出现一过性肝、肾功能异常,经临床研究型MDT团队讨论并根据临床试验方案中的药物不良反应处理原则,予以及时对症处理,未影响后续手术治疗。
1.病例报告
病例1,女,31岁,因“右侧下颌牙龈肿痛伴刷牙出血1周”就诊,抗炎治疗无效,伴右侧下颌牙龈局部肿块形成,经活检证实为高分化鳞癌。患者一般状况良好。右侧下颌牙龈颊侧,自第二磨牙远中至第一前磨牙近中可见“菜花样”肿块,不活动,触之疼痛。肿块上及龈缘,向下越过前庭沟底至颊黏膜,舌侧牙龈未见明显异常。舌无麻木,伸舌无偏斜。颏下、双侧下颌下、双侧颈部未及明显肿大淋巴结。
辅助检查:颌面部MR增强检查提示右侧下颌骨颊侧软组织增厚影,形态不规则,边界不清,大小约24mm×8mm。肿瘤浸润深度11mm,T1I呈等信号,T2WI压脂呈高信号,增强呈明显强化。邻近骨质结构未见破坏。右侧颈Ib区见一直径约7mm淋巴结(图1)。
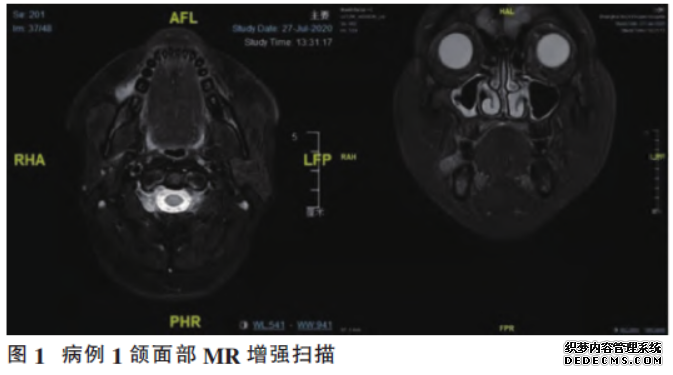
放射学诊断:右侧下颌骨颊侧软组织增厚强化,恶性可能。外院活检病理经本院会诊:“牙龈”黏膜高分化鳞癌。临床分期:cT3N0M0。患者于7月29日至8月26日接受3个周期的卡瑞利珠单抗联合阿帕替尼治疗。7月29日接受第1周期的卡瑞利珠单抗注射,并开始口服阿帕替尼。8月18日化验检查显示胆红素升高,经MDT讨论,停用阿帕替尼,予天晴甘平100mg(口服,每天3次)。
8月28日复查各项指标提示好转,继续服用阿帕替尼。新辅助治疗结束后1周,即9月8日复查颌面部MR:右侧下颌骨颊侧见软组织增厚影,形态不规则,边界不清,大小约23mm×8mm。肿瘤浸润深度9mm,T1I呈等信号,T2WI压脂呈高信号,增强呈明显强化。邻近骨质结构未见破坏。颈部未见直径大于1cm的淋巴结影,较前片范围相仿。9月11日手术治疗,
病例2,男,55岁,因“右侧舌破溃伴疼痛3个月余”就诊,伴疼痛及舌体运动障碍、进食困难。否认舌体麻木。病理检查报告为低分化鳞癌。患者一般状况尚可。右侧舌缘近右侧下颌磨牙区对应处可及菜花状溃疡面,基底质硬,触诊疼痛。口内未及明显肿物。双侧下颌下及颈部未及肿大淋巴结。辅助检查:颌面MR增强提示右侧舌恶性占位,累及口底,大小约33mm×20mm×43mm。肿瘤浸润深度19mm,右侧颈部II区淋巴结转移,右侧下颌下腺阻塞性炎症可能(图2)。
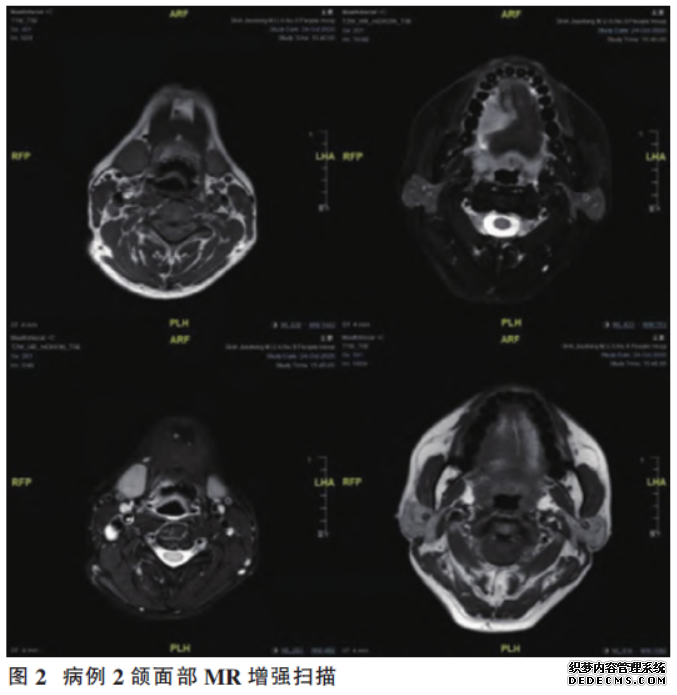
临床分期:cT3N1M0。患者于10月30日至11月26日接受3个周期卡瑞利珠单抗联合阿帕替尼新辅助治疗。12月8日复查颌面MR:右侧舌恶性占位,累及口底,大小约16mm×14mm×16mm。肿瘤浸润深度9mm,右侧颈部Ⅱ区淋巴结转移,较2020-10-24缩小。于12月11日接受手术治疗。术后病理检查报告:“右侧舌、口底”黏膜及软组织慢性炎症,表面上皮局部乳头瘤样增生,固有层炎症细胞浸润,未见明显肿瘤残留。送检切缘阴性;送检淋巴结:右侧颈部Ⅱ区1/16个淋巴结中心变性坏死,考虑为肿瘤新辅助治疗后完全消退,组织细胞浸润;Ⅲ区1/15个淋巴结阳性(+),Ⅰ区8个、Ⅳ区11个、Ⅴ区10个淋巴结均阴性(-)。
2.结果
病例1术后接受常规术后放疗60Gy,后进入随访阶段。现随访17个月,患者健在,无肿瘤复发或转移。病例2术后行常规放疗60Gy,随访至今14个月,患者健在,无肿瘤复发或转移。
3.讨论
3.1局部晚期口腔鳞癌新辅助治疗进展
新辅助治疗是针对无远处转移恶性肿瘤患者在局部治疗前进行的全身性治疗,主要目的是缓解症状、减少肿瘤负荷、争取最大程度获得阴性切缘、增加肿瘤根治机会、降低远处转移等。国内外均有报道称术前新辅助治疗在局部晚期口腔鳞癌治疗中有一定价值,但能否提高患者生存率尚不明确,相关的前瞻性临床研究仍有必要。目前,可切除的局部晚期口腔鳞癌的主要治疗手段是以手术为主的综合序列治疗。
一项新辅助化疗对口腔鳞癌生存率的meta分析显示,在口腔鳞癌序列治疗中,新辅助化疗对提高口腔鳞癌患者生存率无明显优势,这与Hill等在1994年的报道相仿。尽管少有直接证据证明新辅助治疗可以整体提升局部晚期口腔鳞癌患者的生存率,但特定的对诱导治疗敏感的患者群体能得到较明显的生存获益。
同时,新辅助治疗在保存器官的生存质量上有可预期的优势,其或能在减少肿瘤负荷的基础上缩小手术范围,利于重要器官如下颌骨的保存。但是,按诱导治疗后负荷进行手术的安全性仍未得到证明。因此,在现有临床试验中,均应完善术后辅助治疗,以确保治疗效果。近年来,新辅助免疫治疗研究也取得了一定进展。目前,在肝细胞癌、胃癌、食管癌等疾病的新辅助免疫治疗中,已有应用以卡瑞利珠单抗为代表的PD-1抑制剂的报道。新辅助免疫治疗联合靶向治疗正在逐渐成为临床研究的新热点。
3.2卡瑞利珠单抗联合阿帕替尼诱导治疗局部晚期口腔鳞癌的理论依据
卡瑞利珠单抗(SHR-1210,艾瑞卡)是国内自主研发的人源化PD-1抑制剂。阿帕替尼(Apatinib,艾坦)是口服小分子TKI(酪氨酸激酶抑制剂),能高选择性竞争抑制血管内皮细胞生长因子受体2(VEGFR-2),从而抑制肿瘤血管生成。另外,阿帕替尼通过抑制PI3K/AKT通路的抑癌作用已被报道。
目前,卡瑞利珠单抗已被国家食品药品监督管理总局批准应用于至少经过二线系统治疗的复发或难治性经典型霍奇金淋巴瘤的治疗。阿帕替尼已被“中国临床肿瘤学会(CSCO)胃癌诊疗指南”列为胃癌三线治疗I级推荐,并证实在胃癌、肺癌、乳腺癌治疗中是安全和有效的。
在一项卡瑞利珠单抗与阿帕替尼联用治疗晚期肝癌、胃癌和胃食管交界癌的临床I期试验中,Ia期观察到4个剂量限制毒性事件(26.7%),其中1个(6.7%)为3级,阿帕替尼的最大耐受R2PD为250mg;在R2PD联合治疗的33例患者中,20例(60.6%)发生3级及以上的不良事件,均能通过调整剂量和应用药物缓解。一些其他的临床试验也有类似数据证明,两药联用的不良反应在可控程度。
从抑癌机制上,卡瑞利珠单抗和阿帕替尼联用疗效已有一些证据,在口腔鳞癌治疗中有可以预测的疗效,且国内已有报道。卡瑞利珠单抗联合阿帕替尼的治疗策略有协同增效作用,可在一定程度上降低卡瑞利珠单抗应用中反应性皮肤毛细血管增生症(RCCEP)的发生率。PD-L1和VEGFR2-TKI联用的抑癌作用已在一些动物实验中得到验证。
3.3新辅助治疗临床优缺点
除可切除的口腔鳞癌外,对于不可切除病例,新辅助治疗临床试验是增加手术、放疗机会的选择。1997年的一项多中心临床研究中,60例不可切除的头颈部鳞癌患者接受方案为
本文报道的病例中,卡瑞利珠单抗是免疫治疗药物,与阿帕替尼联用有协同增效作用,虽然生存率还待随访观察,但病例2病理缓解率达pCR,该患者有可以预期的生存获益。新辅助治疗的另一优点是能采集术前、术后病理标本,有利于发现新的生物标志物,对筛选敏感患者、选用新药都有积极意义。由于口腔鳞癌大多位置表浅,利于术前病理标本采集,为前瞻性研究提供了有利条件。因此,新辅助治疗在生物标志物的筛选方面大有可为。
不可忽视的是,上述研究中提到,与临床Ⅰ/Ⅱ期相比,在局部晚期口腔鳞癌新辅助化疗中,不良反应发生率似乎更高。亦有前瞻性临床试验提示,新辅助化疗不仅不能使患者的总生存率获得提高,还面临不容小觑的不良反应和毒副作用,这对临床试验的设计者提出了更高的要求。将MDT模式用于此类临床实践中,能实现临床操作的设计、实施、记录、评估的规范化。
3.4临床应用注意事项
将MDT模式结合到临床实践中,可以及时更换治疗方案。病例1在临床试验过程中出现一过性胆红素升高,肝、肾功能异常,而肝功能异常是卡瑞利珠单抗应用和阿帕替尼应用中常出现的不良反应。来自10项共计1116例卡瑞利珠单抗单药治疗的临床研究的安全性数据显示,血胆红素升高出现率为11.5%,为最常见不良反应的第7位;同时为最常见的≥3级不良反应的第3位(3.0%)。
在一项阿帕替尼(甲磺酸阿帕替尼)用于晚期胃癌的临床Ⅲ期多中心、随机、安慰剂对照试验(n=267)中,药物的肝脏毒性包括服药后转氨酶、胆红素、碱性磷酸酶、r谷氨酸转肽酶、乳酸脱氢酶升高等,且多数肝酶异常在服药后第三周期开始发生。本例患者自7月29日开始接受卡瑞利珠单抗联合阿帕替尼治疗,在8月18日出现血胆红素升高。
经MDT讨论后,停用阿帕替尼并予天晴甘平,停药后好转,肝、肾功能恢复后继续服药至疗程结束。不良事件为CTCAE3级,与试验药可能有关。MDT模式用于本例患者的诊治,为临床试验中不良事件提供了规范、标准化的诊治和报告流程。
综上所述,新辅助治疗作为局部晚期口腔鳞癌综合序列治疗研究中的重要一环,能使部分患者获得可预期的获益。利用生物标志物筛选部分合适患者,可能是今后新辅助治疗研究的方向之一。新辅助治疗也面临一些局限,如可能延误手术时机、不良反应和毒副作用等,有待于研究解决。
来源:张益益,杨玥怡,琚梧桐,钟来平.局部晚期口腔鳞癌新辅助免疫靶向治疗2例及文献复习[J].中国口腔颌面外科杂志,2022,20(04):413-416.
 纵隔大细胞神经内分泌癌1例CT影像
纵隔大细胞神经内分泌癌1例CT影像  张力性纵隔气肿影像表现及严重度分级
张力性纵隔气肿影像表现及严重度分级 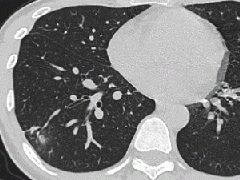 迅速增大的肺部结节,首先考虑良性,确诊需要肺穿
迅速增大的肺部结节,首先考虑良性,确诊需要肺穿 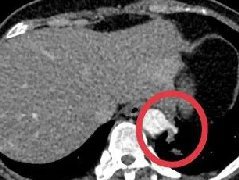 肺隔离症:易误诊为肺癌的占位性病变,肺穿刺禁忌!
肺隔离症:易误诊为肺癌的占位性病变,肺穿刺禁忌! 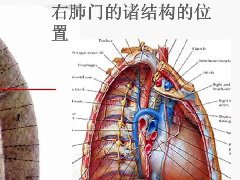 肺段与肺内管道应用解剖
肺段与肺内管道应用解剖 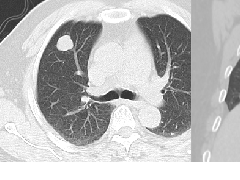 肺转移瘤的十种不典型CT表现
肺转移瘤的十种不典型CT表现 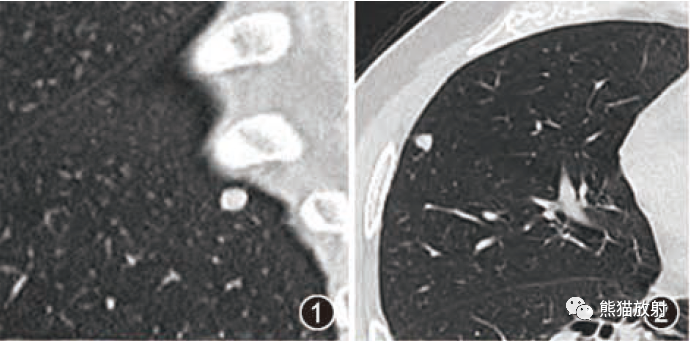 肺内淋巴结的CT表现特点及与病理对照
肺内淋巴结的CT表现特点及与病理对照  肺实变与肺不张的CT鉴别诊断
肺实变与肺不张的CT鉴别诊断  医生现身说法,这五种忙帮不得!
医生现身说法,这五种忙帮不得!  北大教授:要真正让医务人员有阳光体面的收入!医
北大教授:要真正让医务人员有阳光体面的收入!医  为值夜班的医生护士鼓与呼:请给我们更多关注!
为值夜班的医生护士鼓与呼:请给我们更多关注!  广东拟取消医院用药数量限制,满足患者多样性需求
广东拟取消医院用药数量限制,满足患者多样性需求  博士、硕士入职就给精装房!又有医院不惜下血本招
博士、硕士入职就给精装房!又有医院不惜下血本招  历时7年之久,温医生宣判无罪!
历时7年之久,温医生宣判无罪!  重磅!四川发文:严禁限制医生多点执业
重磅!四川发文:严禁限制医生多点执业  与真人医生诊断一致性达96%:AI医生应用前景广阔
与真人医生诊断一致性达96%:AI医生应用前景广阔 
