作者:凌海平,杭春华,那世杰,庄宗,刘涛,戴嵬,张庆荣,南京大学医学院附属鼓楼医院神经外科
胼胝体动静脉畸形是临床较为少见的一类
1.资料与方法
1.1 研究对象
6例中,男2例,女4例;年龄16~35岁,平均(27.17±6.31)岁。6例均以
1.2 影像学评估
术前完善头颅CT或MRI检查,了解病变的部位、范围、畸形团的特点等。术前均进行全
1.3 治疗方法
经术前影像学评估后,采用Seldinger法穿刺右侧股动脉,置入6F导管鞘。治疗时,全身
注胶过程中,关注胶反流情况和向畸形团弥散情况。如果出现胶过度反流或向引流静脉弥散,停止注胶,观察等待,重新注胶。术后造影,必要时行3D造影,判断栓塞情况;并行XPer
1.4 预后评估
术后即刻及术后半年随访,复查造影评估栓塞情况,采用改良Rankin 量表(modified Rankin scale,mRS)评分评估预后情况。
2.结果
2.1 治疗结果
术后即刻造影显示大部分栓塞3例,完全栓塞3例。围手术期未发生
2.2 典型病例
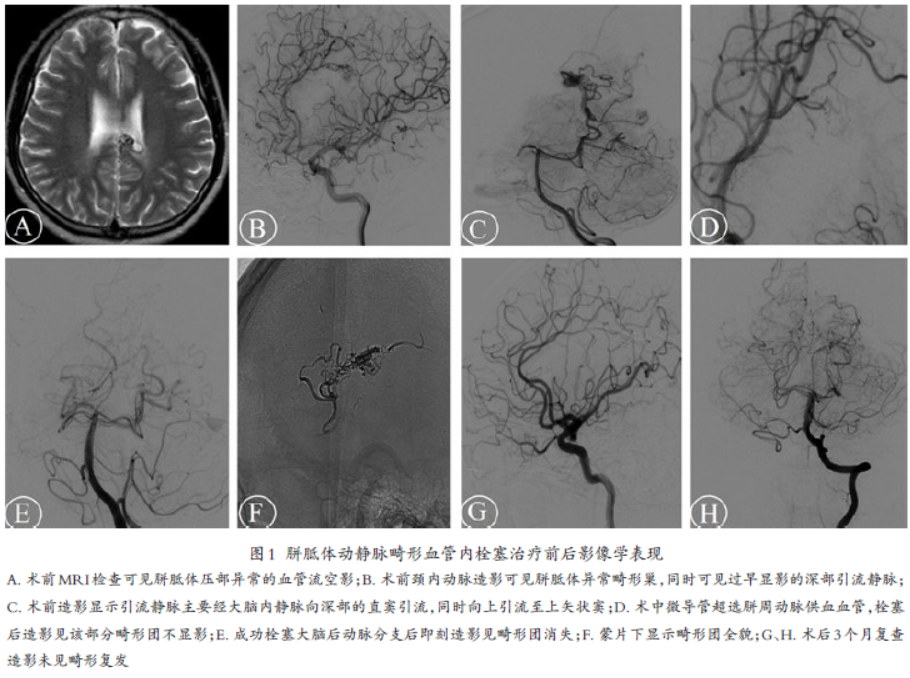
29岁女性,2014年9月因自发性脑室出血、蛛网膜下腔出血就诊于外院,对症治疗后出院。2020年8月13日因自发性脑出血术后5年余就诊于我院。入院后MRI、DSA检查示胼胝体动静脉畸形,主要由左侧胼周动脉及左侧大脑后动脉分支供血,引流静脉分别向上矢状窦及大脑内静脉引流(图1A~C)。
2020年8月18日行胼胝体动静脉畸形栓塞术,术中分别经左侧大脑前动脉的胼周动脉及左侧大脑后动脉-胼周动脉完全栓塞动静脉畸形(图1D~F)。2020年11月5日复查脑血管造影未见明确畸形复发(图1G、1H)。
3.讨论
胼胝体动静脉畸形的人群发病率在1.1%~3%,住院病人发生率在6.7%~14.8%,占脑动静脉畸形的8~9%。Yasargil等将胼胝体动静脉畸形按累及部位分为膝部、体部、压部以及累及全胼胝体四种类型。胼胝体动静脉畸形以胼胝体压部更多见。胼胝体供血动脉来源较为复杂,膝部主要以胼周动脉分支或胼缘动脉分支为主,体部、压部可来源于胼周动脉、后胼周动脉、大脑后动脉分支、脉络膜后动脉。
由于供血动脉可能分别来自前、后循环,因而栓塞术中需要评估在不同供血动脉上的返流及栓塞程度,可行双侧股动脉穿刺,分别置入造影导管及导引导管,同时评估前、后循环供血的栓塞情况。
胼胝体动静脉畸形出血发生率高,可能的原因包括:胼胝体动静脉畸形多为小型病灶,供血动脉多位远端细小分支血管,畸形团体积较小,血流量相对较低,血流阻力增大,这可能是这类动静脉畸形易于出血的原因;其次,多为单一的深静脉引流,单一的深静脉引流,引流静脉易出现成角及狭窄,同时大脑内静脉需接受正常的脑深部静脉回流,进一步限制畸形团的静脉回流,容易诱发动静脉畸形出血;再次,病灶位置深在、靠近侧脑室,缺乏脑组织支撑,也可能是其易发生出血的原因。
胼胝体动静脉畸形主要由远端分支血管供血,供血动脉管腔纤细、血管迂曲、走行距离长,这导致栓塞术中存在导管超选较为困难,需要管径更细小的导管才易于超选。本文病例所使用的微导管为Marathon微导管(1.5F)或Apollo导管(1.5F)。这两款微导管对于纤细、迂曲的血管均具有良好的通过性。
对于走行更远及迂曲的纤细血管,Apollo微导管可能不合适,因为Apollo微导管在解脱点处的管腔会增粗,同时纤细血管对导管有限制作用。此时,可选用Marathon微导管,其头端可塑形,也可以易于通过迂曲血管。如果供血动脉纤细,术中需要很好地控制生物胶的返流长度,返流过长会增加拔管的难度以及增加血管损伤导致出血的风险。
本文5例选择使用Onyx胶,1例使用Glubran胶。Onyx胶的优势在于允许返流的距离更长,同时具有较好的弥散性,尽管Onyx胶为非粘性液体栓塞剂,术中允许等待的时间更长,但在过于纤细的供血动脉内仍有可能造成拔管困难。本文1例术中因供血动脉纤细、术中液体栓塞剂反流过长,导致拔管困难而留置导管在病人体内。因此,对需要较大程度栓塞动静脉畸形,且预计需要较长返流的供血动脉的栓塞,可解脱导管可能是一个很好的选择。
本文3例使用可解脱微导管,其优势在于允许更长距离的返流,拔管时更加安全。本文多数病人存在多根供血动脉,我们的经验是可先利用Marathon微导管栓塞非主要供血动脉及部分畸形团,再利用可解脱微导管尽可能地栓塞动静脉畸形。这样可以有效降低术中因过度栓塞出现静脉闭塞诱发畸形团出血的风险,也可以减少拔管困难。术前应充分评估,选择走行距离短、迂曲程度小及管腔大小合适的供血动脉做为主要栓塞通路,为了允许更大限度的反流,可在这类供血动脉的栓塞过程中使用可解脱微导管。
术中适当长度的反流可对供血动脉形成“阻断效应”,促使栓塞剂向畸形团内弥散,最大范围地栓塞动静脉畸形。胼胝体动静脉畸形术后出现神经功能障碍更多见于开放手术,且胼胝体压部动静脉畸形术后更易出现。胼胝体内存在大量的联络纤维,神经功能障碍的出现可能由于开放手术损伤了胼胝体内的联络纤维。同时胼胝体周围毗邻丘脑、扣带回等结构,因而胼胝体动静脉畸形术后也可因毗邻脑组织损伤导致神经功能障碍。但血管内治疗后出现神经功能障碍的报道非常少见。
本文2例术后出现
总之,胼胝体动静脉畸形临床少见,以小型病灶多见、多深部静脉引流、位于深部脑室旁等,出血风险高,临床出血病例多见,因而需要积极干预。由于胼胝体的特殊解剖位置,血管内治疗具有良好的适应证,是一种非常安全和有效的治疗手段。
来源:凌海平,杭春华,那世杰,庄宗,刘涛,戴嵬,张庆荣.胼胝体动静脉畸形的血管内治疗的疗效分析[J].中国临床神经外科杂志,2022,27(01):28-30+50.
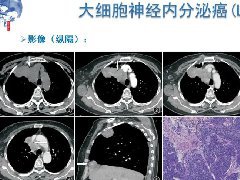 纵隔大细胞神经内分泌癌1例CT影像
纵隔大细胞神经内分泌癌1例CT影像 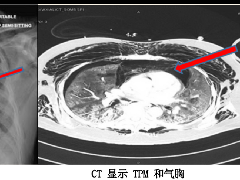 张力性纵隔气肿影像表现及严重度分级
张力性纵隔气肿影像表现及严重度分级 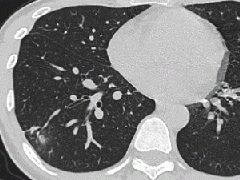 迅速增大的肺部结节,首先考虑良性,确诊需要肺穿
迅速增大的肺部结节,首先考虑良性,确诊需要肺穿 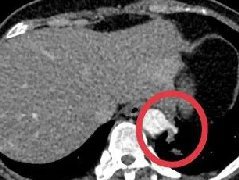 肺隔离症:易误诊为肺癌的占位性病变,肺穿刺禁忌!
肺隔离症:易误诊为肺癌的占位性病变,肺穿刺禁忌! 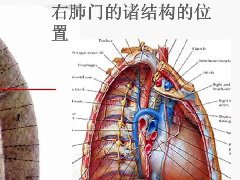 肺段与肺内管道应用解剖
肺段与肺内管道应用解剖 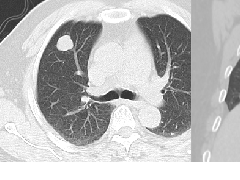 肺转移瘤的十种不典型CT表现
肺转移瘤的十种不典型CT表现 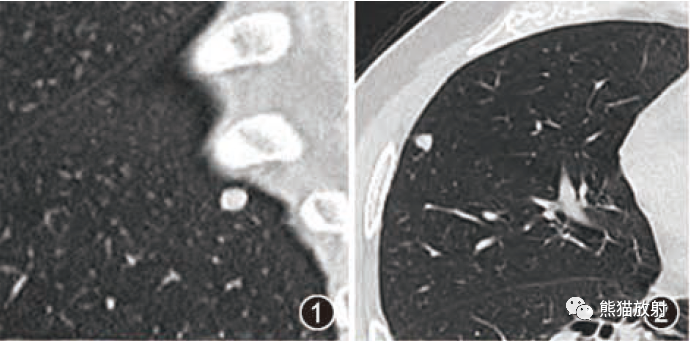 肺内淋巴结的CT表现特点及与病理对照
肺内淋巴结的CT表现特点及与病理对照  肺实变与肺不张的CT鉴别诊断
肺实变与肺不张的CT鉴别诊断  医生现身说法,这五种忙帮不得!
医生现身说法,这五种忙帮不得!  北大教授:要真正让医务人员有阳光体面的收入!医
北大教授:要真正让医务人员有阳光体面的收入!医  为值夜班的医生护士鼓与呼:请给我们更多关注!
为值夜班的医生护士鼓与呼:请给我们更多关注!  广东拟取消医院用药数量限制,满足患者多样性需求
广东拟取消医院用药数量限制,满足患者多样性需求  博士、硕士入职就给精装房!又有医院不惜下血本招
博士、硕士入职就给精装房!又有医院不惜下血本招  历时7年之久,温医生宣判无罪!
历时7年之久,温医生宣判无罪!  重磅!四川发文:严禁限制医生多点执业
重磅!四川发文:严禁限制医生多点执业  与真人医生诊断一致性达96%:AI医生应用前景广阔
与真人医生诊断一致性达96%:AI医生应用前景广阔 
